سمن صبری / هلیا بهشتی فر
آزمایشگاه شیمی عمومی
در علم شیمی، محلول به ترکیب همگن دو یا چند ماده گفته میشود. در حل کردن مادهای در ماده دیگر، یکی از مواد حلشونده و دیگری حلال خوانده میشود. برای مثال آبنبات (حل شونده) در هنگام خوردن در بزاق دهان (حلال) حل میشود. یا ممکن است که مایعی در مایع دیگر حل گردد و یا گازی با گازی دیگر ترکیب گردد. تمام محلولها بر اساس فعل و انفعالات بین مولکولها و یونهای حلال و حلشونده طبقه بندی میشوند و در نتیجه از انرژی آزاد مولکولهای مواد کم میشود.
منظور از ترکیب همگن این است که اجزای تشکیل دهنده ی مخلوط در یک فاز باشند. خواص مخلوط (غلظت، دما، چگالی و ...) به طور یکنواخت در حجم مخلوط هستند. به طور معمول ماده ای که به مقدار بیشتری در مخلوط موجود باشد، حلال نامیده می شود. حلال می تواند گاز، مایع و یا جامد باشد. به مواد دیگری که در محلول موجود هستند(به غیر از حلال) حل شونده می گویند. حلال در هر فاز فیزیکی باشد، محلول هم در همان فاز خواهد بود.
محلولی را استاندارد می گویند که در آن ، رابطه بین مقادیر ماده حلشده و محلول یا رابطه بین مقدار ماده حلشده و حلال بنحوی معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکیل دهنده محلول ، غلظت محلول مشخص میگردد. بسیاری از واکنشها در حالت محلول انجام میشوند و محاسبههای کمی برای اینگونه واکنشها بر مبنای غلظت آنها صورت میگیرد. برای بیان غلظت ، روشهای گوناگونی وجود دارد و محلولهای استاندارد را براساس غلظت بیان میکند.
سمن صبری / هلیا بهشتی فر
آزمایشگاه شیمی عمومی
جداسازی اجزاء یك مخلوط:
در بیشتر مواقع لازم است كه اجزاء یك مخلوط را از هم جدا كنیم. برای تهیه آب شیرین نمك و سایر املاح را از آب جدا می كنند . فراورده های نفتی هم بصورت مخلوط با یكدیگر تحت عنوان نفت خام یافت می شوند.
زمانی می توان اجزاء یك مخلوط را از هم جدا كرد كه اجزاء حداقل در یك ویژگی با هم اختلاف داشته باشند.
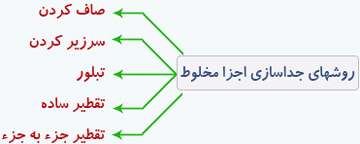
الف) صاف كردن:
از این روش هنگامی استفاده می شود كه اجزاء مخلوط از نظر اندازه ذرات با هم تفاوت داشته باشند. الك كردن آرد، جداكردن شن و ماسه از یكدیگر، جداكردن تفاله از چای نمونه هایی از صاف كردن هستند.
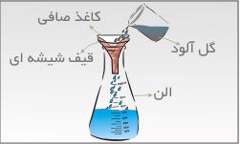
ب) سرریز كردن:
هنگامی از این روش استفاده می شود كه یك جزء از جزء دیگر سبك تر باشد. اگر مخلوط آب روغن بی حركت بماند چون روغن از آب سبك تر است بر روی آب قرار می گرید و می توان با سر ریز كردن و یا با استفاده از وسیله مقابل كه قیف جدا كننده یا قیف دكانتور نامیده می شود آن ها را از هم جدا كرد.
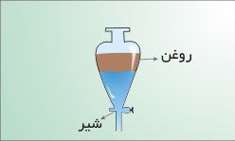
ج) تبلور:
از روش تبلور برای جدا كردن جزء جامد از مایع استفاده می شود . اگر مخلوط جامد در مایعی مانند آب نمك را سرد كنیم از آنجا كه انحلال پذیری با كاهش دما كم می شود مقداری از حل شونده بصورت بلور در ته ظرف ته نشین می شود .
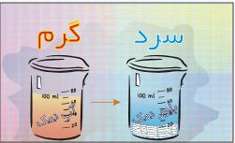
د) تقطیر ساده:
ه) تقطیر جزء به جزء:
از این روش برای جدا كردن اجزاء مخلوط چند مایع كه نقطه جوش متفاوت دارند استفاده می شود اجزاء نفت خام را به همین روش از هم جدا می كنند. به این ترتیب كه نفت خام را تا ٤٠٠ درجه سانتیگراد حرارت می دهند تا بسیاری از اجزاء آن به جوش آیند و به صورت بخار در آیند. نفت خام حرارت داده شده را به قسمت پایین دستگاهی به نام برج تقطیر می فرستند بخارات حاصل هنگام صعود از دستگاه به سینی های نصب شده برخورد كرده و بر اساس تفاوت نقطه جوش به مایع تبدیل و از هم جدا می شوند.
سمن صبری و هلیا بهشتی فر
آزمایشگاه شیمی عمومی
 |
نگاه کلی
جیوه ، تنها فلز مایع در دمای معمولی است و بخاطر این خاصیت ، کاربردهای فراوانی در صنعت ، پزشکی و صنایع روشنایی دارد. جیوه از تمام فلزات ، فرّارتر و بخار آن کاملا سمی است. جیوه از ششها به جریان خون نفوذ کرده ، سپس از سد خون و مغز گذشته و با وارد شدن به مغز ، آسیب شدیدی به سیستم اعصاب مرکزی میرساند.
راههای وارد شدن جیوه به محیط زیست
جیوه در نتیجه سوزاندن زغال سنگ و مازوت که دارای مقادیر کمی جیوه هستند، بصورت بخار وارد جَو میشود. همچنین از خاکستر کردن ضایعات جامد مانند باتریهای مستعمل که دارای جیوه هستند در محیط زیست رها میشود. از طرف دیگر ، جیوه بطور گسترده در صنایع مختلف مانند صنایع الکترونیک ( سوئیچ الکتریکی و لامپهای بخار جیوه ) و همچنین در استخراج فلزات قیمتی ، استفاده و از این طریق وارد جو میشود.
این منبع جیوه جوی ، امروزه رقیب مواد خروجی از آتشفشانهاست که قبلا منبع عمده جیوه معلق در هوا محسوب میشدند. جیوه در هوا اکثرا به شکل گاز است و مقدار اندکی از آن ، به ذرههای معلق متصل است. جیوه گازی معلق در هوا است که میتواند مسافتهای زیادی را قبل از رسوب در خاک و آبراههها طی کند.
کاربردهای جیوه در صنعت
ملغمه جیوه
ملغمه ، آلیاژ جیوه با فلزات یا ترکیبات فلزی است. بهعنوان مثال ، ملغمه دندان که برای پر کردن دندان بکار میرود، آلیاژی به نسبت برابر از جیوه مایع و مخلوطنقره و قلع است. از ملغمه جیوه از سال 1570 تا سال 1900 برای استخراج نقره استفاده میشد که به ازای هر گرم نقره ، یک گرم جیوه وارد جَو میکرد. امروزه هم در برخی کشورها برای استخراج طلا از ملغمه جیوه استفاده میکنند، به این ترتیب که با افزودن جیوه به خاک معدنی که حاوی مقدار کمی طلا یا نقره است، با تشکیل ملغمه آنرا استخراج کرده و سپس با گرم کردن ، جیوه را تبخیر میکنند.
این روش به آلودگی هوا و محیط زیست میانجامد و برای سلامتی کارگرانی که در معرض بخار حاصل از ملغمه قرار میگیرند، مضر است. احتمالا بخاطر سمّیت بخار جیوه بود که بردگانی که در معادن شنگرف (HgS) رومیها کار میکردند، بعد از 6 ماه میمردند.
جیوه و فرایند کلر - قلیا
در برخی از کارخانجات کلر - قلیا که از طریق الکترولیز محلول آبی ، سدیم کلرید را به محصولات تجاری کلروهیدروکسید تبدیل میکنند، ملغمهای از سدیم و جیوه را بکار میبرند. سدیم وقتی در ملغمه جیوه حل میشود، از میزان واکنشپذیری آن نسبت به سدیم آزاد کاسته میشود، بطوریکه سدیم بسیار واکنشپذیر با آب ، بصورت ملغمه Hg - Na با آب واکنش نمیدهد. از طریق سدیم ، هیدروکسید عاری از نمک بدست میآورند و جیوه را بازیابی و مجددا به سلول اصلی بر میگردانند.
اما به هر حال ، بازیافت جیوه کامل نیست و مقداری از آن به هوا یا به رودخانهای که آب مورد نیاز خنک کردن دستگاهها از آن تامین میشود، راه مییابد. امروزه در کشورهای صنعتی برای جدا کردن محلول NaCl از محلول عاری از کلرید از الکترودهای غشایی شناساگر فلزی (حساس به 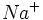 ) استفاده میشود.
) استفاده میشود.
جیوه یونی
یون مرکوریک ( 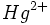 ) در پساب کارخانجات کلر - قلیا وجود دارد. مهمترین کانی جیوه عینی ، HgS ، نمک بسیار نامحلول در آب است و برای بهسازی پساب کارخانجات با افزودن نمک محلول
) در پساب کارخانجات کلر - قلیا وجود دارد. مهمترین کانی جیوه عینی ، HgS ، نمک بسیار نامحلول در آب است و برای بهسازی پساب کارخانجات با افزودن نمک محلول  ، یون جیوه را بصورت HgS رسوب میدهند. نمک نیترات
، یون جیوه را بصورت HgS رسوب میدهند. نمک نیترات 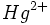 در آب حل میشود و زمانی برای آمادهسازی خز جهت ساختن کلاه نمدی بکار میرفت. در نتیجه کارگران کلاه دوزی ، اغلب دچار ناهنجاریهای عصبی مانند لرزش ماهیچه ، افسردگی ، فراموشی و . . . میشدند.
در آب حل میشود و زمانی برای آمادهسازی خز جهت ساختن کلاه نمدی بکار میرفت. در نتیجه کارگران کلاه دوزی ، اغلب دچار ناهنجاریهای عصبی مانند لرزش ماهیچه ، افسردگی ، فراموشی و . . . میشدند.
بخار جیوه به سیستم اعصاب مرکزی حمله میکند. اما هدف اصلیاش 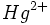 کلیهها و کبد است. مرکوریک اسید (HgO) که در باتریهای معمولی چراغ قوه برای جلوگیری از خورده شدن الکترود روی استفاده میشود، بعد از سوزاندن باتریهای مصرف شده ، آزاد و وارد جو میشود که منبع اصلی آلودگی محیط زیست است.
کلیهها و کبد است. مرکوریک اسید (HgO) که در باتریهای معمولی چراغ قوه برای جلوگیری از خورده شدن الکترود روی استفاده میشود، بعد از سوزاندن باتریهای مصرف شده ، آزاد و وارد جو میشود که منبع اصلی آلودگی محیط زیست است.
 |
نمکهای متیل جیوه
متیل جیوه بعد از بخار جیوه خطرناکترین شکل جیوه است. متیل جیوه نسبت به نمکهای 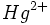 سمّ قویتری است، زیرا در بافت چربی حیوانات ، انحلالپذیر است و در آنجا تجمع و بزرگنمایی زیستی دارد. همچنین میتواند از سد خون ، مغز و از سد جفت جنین انسان عبور کند. فرایند متیلدار شدن جیوه در تهنشستهای گلآلود رودخانهها و بویژه در شرایط ناهوازی توسط متیل کبالامین صورت میگیرد. بیشتر جیوه موجود در بدن انسان بصورت متیل جیوه است و بیشتر از طریق خوردن ماهی وارد بدن انسان میشود.
سمّ قویتری است، زیرا در بافت چربی حیوانات ، انحلالپذیر است و در آنجا تجمع و بزرگنمایی زیستی دارد. همچنین میتواند از سد خون ، مغز و از سد جفت جنین انسان عبور کند. فرایند متیلدار شدن جیوه در تهنشستهای گلآلود رودخانهها و بویژه در شرایط ناهوازی توسط متیل کبالامین صورت میگیرد. بیشتر جیوه موجود در بدن انسان بصورت متیل جیوه است و بیشتر از طریق خوردن ماهی وارد بدن انسان میشود.
از منابع دیگر متیل جیوه میتوان ترکیبات آلی جیوه را که بصورت قارچکشها در کشاورزی استفاده میشود، نام برد که در نتیجه تماس با خاک این ترکیبات شکسته شده و جیوه با اتصال به گروههای گوگرددار در خاکهای رس و ماده آلی بصورت ترکیبهای نامحلول به دام میافتد.
استفاده از متیل جیوه بهعنوان قارچکش برای محافظت دانهها سبب کاهش قابل ملاحظه پرندگانی شد که از این دانهها مصرف کرده بودند و همچنین صدها مرگ در عراق و آمریکا از مصرف نانی که دانههای گندم آن با متیل جیوه در تماس بوده گزارش شده است.
سمّیت متیل جیوه
نیم عمر ترکیبات متیل جیوه در انسان حدود 70 روز طولانیتر از نمکهای 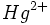 است. در نتیجه متیل جیوه میتواند در بدن با غلظت بیشتری تجمع یابد. علائم بیماری در انسان از معلولیت سیستم اعصاب مرکزی ناشی میشود. این علائم شامل بیحسی دست و پا و تار شدن دید چشم و کوری و از دست دادن حس شنوایی و ... است. بچههای متولد شده از مادرانی که حتی به مقدار کم توسط جیوه مسموم شده باشند، دچار آسیبهای مغزی میشوند.
است. در نتیجه متیل جیوه میتواند در بدن با غلظت بیشتری تجمع یابد. علائم بیماری در انسان از معلولیت سیستم اعصاب مرکزی ناشی میشود. این علائم شامل بیحسی دست و پا و تار شدن دید چشم و کوری و از دست دادن حس شنوایی و ... است. بچههای متولد شده از مادرانی که حتی به مقدار کم توسط جیوه مسموم شده باشند، دچار آسیبهای مغزی میشوند.
از مهمترین عوارض جیوه میتوان به مسمومیت هزاران نفر و مرگ صدها تن از مردم میناماتای ژاپن بخاطر استفاده از ماهی آلوده به جیوه اشاره کرد که این ماهیها توسط پساب یک کارخانه شیمیایی که به خلیج میناماتای میریخت ، آلوده شده بودند ( از 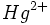 بهعنوان کاتالیزور جهت تولید پلیوینیل کلرید استفاده میکردند.)
بهعنوان کاتالیزور جهت تولید پلیوینیل کلرید استفاده میکردند.)
محلول سازی از محلول های غلیظ آزمایشگاه معمولاً در آزمایشگاه محلولها به صورت غلیظ و با درصد خلوص مشخص و استانداردی وجود دارد و برای تهیه محلول های رقیق تر باید از آن ها استفاده کرد. برای این کار از روابط رقیق سازی استفاده می کنیم : در رابطه بالا نیاز است که نرمالیته یا مولاریته محلول غلیظ موجود در آزمایشگاه را تعیین کنیم. برای تعیین نرمالیته از فرمول زیر استفاده می کنیم : نرمالیته محلول غلیظ را بدست آوردیم. در رابطه اول فقط حجم محلول غلیظ (v2) مجهول است که محاسبه می شود و فقط کافی است این مقدار (v1) را از محلول غلیظ برداشته و به حجم مورد نظر (v2) برسانیم. برای تعیین نرمالیته و مولاریته محلول های آزمایشگاهی می توانید از جدول زیر استفاده کنید. که در این صورت فقط به رابطه اول نیاز خواهید داشت. نام محلول چگالی نرمالیته مولاریته اسید استیک %99.5 1.05 17.5 17.5 اسید سولفوریک %98 1.84 36.8 18.4 اسید نیتریک %70 1.42 15.8 15.8 اسید هیدروکلریدریک%40 1.13 22.6 22.6 اسید هیدروکلریدریک %36 1.18 11.65 11.65 اسید هیدروکلریدریک%32 1.16 10.2 10.2 اسید پرکلریک %70 1.67 11.6 11.6 اسید پرکلریک%60 1.54 9.2 9.2 آمونیاک%35 0.88 18.1 18.1 آمونیاک %25 0.91 13.4 13.4 سدیم هیدروکسید %47 1.50 17.6 17.6 تذکر: در مورد اسیدهای غلیظ و قوی مثل اسید سولفوریک همیشه اسید را به آب اضافه می کنیم. (قبل از اضافه کردن اسید مقداری آب مقطر در بالون بریزید و سپس اسید را اضافه کنید). محلول سازی از مواد جامد آزمایشگاه فقط کافی است مقدار ماده جامد بدست آمده را در مقداری آب مقطر حل کرده و به حجم مورد نظر برسانید. تذکر : در مورد برخی مواد جامد که رطوبت جذب می کنند باید دقت شود که از فرمول نوشته شده بر روی برچسب ظرف ماده جرم مولکولی محاسبه شود. مثلاBaCl2 . 2H2O به جرم مولکولی آن دو ملکول آب (36gr) اضافه شده است که باید در محاسبات لحاظ شود.
| محلول سازی |
|
معمولا براي کار در آزمايشگاه از محلولهاي استاندارد استفاده ميکنند. محلولي را استاندارد مي گويند که در آن ، رابطه بين مقادير ماده حلشده و محلول يا رابطه بين مقدار ماده حلشده و حلال بنحوي معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکيل دهنده محلول ، غلظت محلول مشخص ميگردد. بسياري از واکنشها در حالت محلول انجام ميشوند و محاسبههاي کمي براي اينگونه واکنشها بر مبناي غلظت آنها صورت ميگيرد.
محلولي را استاندارد مي گويند که در آن ، رابطه بين مقادير ماده حلشده و محلول يا رابطه بين مقدار ماده حلشده و حلال بنحوي معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکيل دهنده محلول ، غلظت محلول مشخص ميگردد. بسياري از واکنشها در حالت محلول انجام ميشوند و محاسبههاي کمي براي اينگونه واکنشها بر مبناي غلظت آنها صورت ميگيرد. براي بيان غلظت ، روشهاي گوناگوني وجود دارد و محلولهاي استاندارد را براساس غلظت بيان ميکند.
محلولهاي استاندارد کاربردهاي زيادي دارند، از جمله در تجزيه هاي تيترسنجي (تيتراسيون) ، واکنشهاي خنثي شدن و واکنشهاي اکسيداسيون-احيا و...
| محلولی را استاندارد می گویند که در آن ، رابطه بین مقادیر ماده حلشده و محلول یا رابطه بین مقدار ماده حلشده و حلال بنحوی معلوم باشد. با معلوم بودن مقدار ماده حلشونده و مقدار حلال تشکیل دهنده محلول ، غلظت محلول مشخص میگردد. بسیاری از واکنشها در حالت محلول انجام میشوند و محاسبههای کمی برای اینگونه واکنشها بر مبنای غلظت آنها صورت میگیرد. برای بیان غلظت ، روشهای گوناگونی وجود دارد و محلولهای استاندارد را براساس غلظت بیان میکند. محلولهای استاندارد کاربردهای زیادی دارند، از جمله در تجزیه های تیترسنجی (تیتراسیون) ، واکنشهای خنثی شدن و واکنشهای اکسیداسیون-احیا و... |
محلولهای استاندارد مورد کاربرد
محلول درصد جرمی
محلولی است که در آن مقداری ماده حلشونده در 100 گرم محلول ، حل شده باشد.در صورت و مخرج باید از یک نوع یکای جرم استفاده شود. یعنی هر دو باید برحسب میلیگرم ، گرم یا کیلوگرم بیان شوند. مثلا ، بر روی بر چسب محلول شست وشوی دهان نوشته می شود: "محلول استریل سدیم کلرید 9/0 درصد برای شستشو". عبارت "سدیم کلرید 9/0 درصد" یعنی در 100 گرم از این محلول 9/0 گرم سدیم کلرید وجود دارد و بقیه آن آب است.
برای محلولهای بسیار رقیق ، معمولا غلظت بر حسب قسمت در میلیون (ppm) بیان میشود.
اگر حلال ، آب باشد و مقدار ماده حلشونده چنان کم باشد که چگالی محلول همچنان g.mL-1 1,0 باقی بماند، در اینصورت رابطه به قرار زیر خواهد بود:
از ppm برای بیان مقادیر بسیار کم کاتیونها و آنیونها در آب دریا ، بدن جانداران ، بافتهای گیاهی و میزان آلایندههای هوا و بطور کلی ، در مواردی که مقدار ماده حلشونده خیلی جزئی باشد، استفاده میشود.
محلول گرم در لیتر (غلظت معمولی-C)
در این محلولها ، مقداری ماده حلشونده در یک لیتر محلول وجود دارد.برای مثال ، اگر در 200 میلیلیتر از محلولی به اندازه 4 گرم پتاسیم کلرید حلشده باشد، غلظت معمولی این محلول ، 20 گرم در لیتر خواهد بود.
محلول مول در لیتر (مولار CM)
غلظت مولار رایجترین روش برای بیان غلظت است و محلول مولار ، محلولی است که در هر لیتر آن ، به اندازه یک مول ماده حلشونده ، حل شده باشد. مانند محلول یک مول بر لیتر لیتیم کلرید که در آن ، یک لیتر محلول دارای یک مول لیتیم کلرید است.محلول مولال (m)
محلولی که در آن یک مول ماده حلشونده در یک کیلوگرم حلال شده باشد، محلول مولال نامیده میشود. از غلظت مولال در مطالعه خواص کولیگاتیو محلولها بکار میرود.برای مثال ، اگر در 200 گرم آب خالص ، 0,03 مول کلرید پتاسیم حل شده باشد، مولالیته محلول عبارت خواهد بود:
محلول نرمال (N)
محلول نرمال ، محلولی است که یک اکی والان گرم ماده حلشونده در یک لیتر آن و یا یک میلیاکیوالان گرم در هر لیتر آن حل شده باشد.- مفهوم اکی والان گرم: مقدار وزن اکی والان مواد مختلف طبق رابطه زیر به دست میآید:
E=M/n
مقدار n برای اسیدها برابر تعداد هیدروژنهای اسیدی و برای بازها ، برابر تعداد -OH ، برای نمکها برابر ظرفیت فلز ضربدر تعداد فلز و برای واکنشهای اکسایش- کاهش برابر درجه کاهش یا اکسایش است.
با بدست آوردن مقدار E (وزن اکی والان) میتوان تعداد اکیوالان را از رابطه زیر حساب کرد:
در نتیجه ، نرمالیته یک محلول بیانگر تعداد اکیوالانها در یک لیتر محلول یا تعداد میلیاکیوالان در هر میلیلیتر محلول میباشد. پس ، یک محلول 0,2 N نقره نیترات ، 0,2 میلی اکی والان (meq) از نقرهنیترات در هر میلیلیتر یا 0,2 اکی والان (eq) در هر لیتر محلول دارد.
روابط بین محلول های استاندارد
در این روابط: CM مولاریته ، C غلظت گرم در لیتر ، N نرمالیته ، M جرم مولکولی ، E اکی والان گرم و n ظرفیت است.
بسمه تعالی
محلول سازی
کار ما در ازمایشگاه بر روی 2 نوع محلول می باشد:
1
قابل توجه دانشجویان گروه مهندسی شیمی
در مورد محلول های استاندارد تحقیقات خود را کامل کنید.
تا تاریخ 25 اسفند گزارش های خود را تکمیل کنید.
موفق باشید
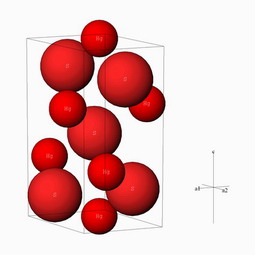
به هر آلیاژی از جیوه، مَلغَمه یا آمالگام (به انگلیسی: Amalgam) گفته میشود. به سخن دیگر ملغمه ترکیب جیوه-فلز است که ممکن است مایع یا جامد باشد. از ملغمهها معمولاً در پر کردن دندان بهره میگیرند. آمالگام دندانی مادهای غیر همرنگ (نقره ای یا سیاه) است که برای پر کردن دندان از آن استفاده میشود و مرکب از 50 درصد جیوه 34.5 درصد نقره ، 9% قلع ، 6% مس و 0.5% روی است.
آمالگام در 3 حالت وجود داره:
مايع, پلاستيك , جامد.
آمالگام هاي مايع، محلول هاي واقعي عناصر آلياژي در جيوه اند.
آمالگام هاي پلاستيک، سوسپانسيون ذرات جامد در جيوه اند و يا اينکه محلول اشباع شده اي از جيوه باشند.
آمالگام هاي جامد، ترکيبات حدواسطي هستند که اغلب با آلياژ کننده ها يا بلورهاي مخلوط اوليه در آميخته اند.
به نام انکه پروانه حیران اوست
ازمایش اول:جامد در مایع(صورت ازمایش:0.2 مولار Nacl را به حجم 50ml برسانید)
که روی ترازو قرار داده ایم و ان را صفر کرده ایم مقدار0.585g نمک طعام(Nacl) که از محاسباتی که درپایین
ذکر خواهد شد بدست اورده ایم با استفاده از قاشقک در بشر مورد نظر می ریزیم و این کار با نهایت دقت انجام شود تا ترازو عدد مورد نظر را نشان دهد سپس در بشر مقدار کمی اب مقطر ریخته و با همزن شیشه ای نمک و اب را هم میزنیم تا کاملا نمک حل شود بعد محلول را در بالون ژوژه 50 ریخته و به وسیله ی ابفشان و بسیار با دقت ان را به حجم می رسانیم یعنی تا خط نشانه ی بالن اب میریزیم و بعد در پوش را می گذاریم و هم میزنیم پس از اتمام ازمایش وسایل شسته و در جای خود گذاشته شود کار به اتمام رسید.
CM=0.2mol/lit
MV=58.5
V=50ml CM=C/MV
0.2=C/58.5
C=11.7g/l
11.7*50/1000=
0.585g Nacl
ابتدا تمام وسایل مورد نیاز در ازمایش را میشوییم و کاملا با یک پارچه خشک می کنیم سپس بشر را روی ترازو قرار میدهیم و ترازو را حتما صفر می کنیم و بعد با استفاده از قاشقک مقدار 0.106g از نمک مورد نظر(Na2Co3) را این مقدار از محاسباتی که در پایین ذکر شده است را برداشته و با دقت بسیار زیاد ان را در بشر ریخته تا ترازو عدد 0.106 را نشان دهد سپس مقدار کمی اب در بشر ریخته و با اشتفاده از همزن شیشه ای هم میزنیم تا نمک بطور کامل در اب حل شده و بعد محلول را در بالن ژوژه ی 100mlریخته و با استفاده از ابفشان و با نهایت دقت ان را به حجم 100 می رسانیم اب را تا خط نشانه می ریزیم و حتما مستقیم به خط نشانه نگاه می کنیم تا ذچار خطای دید نشویم و بعد در پوش را می گذاریم پس از اتمام ازمایش وسایل شسته و خشک شود ودر جای خود گذاشته شود کار به اتمام رسید.
M V=106
V=100ml
CM=C/MV
0.01=C/106
C=1.06g/l
1.06*100/1000=
0.106g Na2Co3
ابتدا وسایل را شسته وبا پارچه خشک می کنیم.برای شروع ازمایش لازم به ذکر است چون در این ازمایش نمونه ی مایع ما اسید است پس تمام مراحل در زیر هود و با نهایت دقت انجام می شود و باید حتما این نکته را در این ازمایش دانست که اب را نباید روی اسید ریخت چون شروع واکنش بین اسید و اب با ازاد کردن مقدار زیادی گرماست که اگر به این نکته توجه نشود خطر انفجار وجود دارد پس با دانستن این نکته به ادامه ی ازمایش می پردازیم در بشر مقداری اب ریخته و بشر را به زیر هود منتقل می کنیم و با استفاده از پیپت مقدار0.83ml از اسید Hcl برداشته که این مقدار از انجام محاسبات زیر بدست امده و در مورد پیپت حتما ان را با انگشت اشاره گرفته و با نهایت دقت از زیر هود بیرون نمی اوریم و مقدار معین را در بشر بر روی اب ریخته و ارام هم می زنیم و بعد محلول بدست امده را با استفاده از قیف به درون بالن ژوژه منتقل میکنیم با نهایت دقت این کار را انجام می دهیم و بعد با استفاده از ابفشان ان را بسیا با دقت به حجم 100 در بالن ژوژه می رسانیم و تا خط نشانه که درست از رو به رو به ان نگاه میکنیم پر می کنیم و بعد در پوش را می گذازیم و به ارامی هم می زنیم محلول ما اماده است پس از انجام ازمایش محلول را به ارامی در ته سینک تخلیه می کنیم و ظرفها را شسته خشک کرده و در جای خود قرار می دهیم کار به اتمام رسید.
CM=10*a*d/MV
CM=10*37*1.19/36.5
CM=12.06
12.06*V1=0.01*100
V1=0.83ml
ابتدا وسایل را شسته وبا پارچه خشک می کنیم.برای شروع ازمایش لازم به ذکر است چون در این ازمایش نمونه ی مایع ما اسید است پس تمام مراحل در زیر هود و با نهایت دقت انجام می شود و باید حتما این نکته را در این ازمایش دانست که اب را نباید روی اسید ریخت چون شروع واکنش بین اسید و اب با ازاد کردن مقدار زیادی گرماست که اگر به این نکته توجه نشود خطر انفجار وجود دارد پس با دانستن این نکته به ادامه ی ازمایش می پردازیم در بشر مقداری اب ریخته و بشر را به زیر هود منتقل می کنیم و با استفاده از پیپت مقدار0.637mlاز اسید H2So4برداشته که این مقدار از انجام محاسبات زیر بدست امده و در مورد پیپت حتما ان را با انگشت اشاره گرفته و با نهایت دقت از زیر هود بیرون نمی اوریم و مقدار معین را در بشر بر روی اب ریخته و ارام هم می زنیم و بعد محلول بدست امده را با استفاده از قیف به درون بالن ژوژه منتقل میکنیم با نهایت دقت این کار را انجام می دهیم و بعد با استفاده از ابفشان ان را بسیا با دقت به حجم 250ml در بالن ژوژه می رسانیم و تا خط نشانه که درست از رو به رو به ان نگاه میکنیم پر می کنیم و بعد در پوش را می گذازیم و به ارامی هم می زنیم محلول ما اماده است پس از انجام ازمایش محلول را به ارامی در ته سینک تخلیه می کنیم و ظرفها را شسته خشک کرده و در جای خود قرار می دهیم کار به اتمام رسید.
MV=98 a=98% d=1.96g/lit
CM=10*98*1.96/98
CM=19.6
CM1*V1=CM2*V2
19.6*V1=0.05*250
V1=0.637ml
CM=10*a*d/MV
نحوه ی انجام محاسبات:
نحوه ی انجام ازمایش:
ازمایش چهارم:مایع در مایع(صورت ازمایش:محلول0.05 مولاربه حجم250ml از H2So4 با a=98% و d=1.96g/lit) وسایل مورد نیاز:بشر-پیپت مدرج-بالن ژوژه ی100ml-درپوش-ابفشان-قیف
CM1*V1=CM2*V2
MV=36.5 a=37% d=1.19g/lit
نحوه ی انجام محاسبات:
نحوه ی انجام ازمایش:
وسایل مورد نیاز:بشر-پیپت مدرج-بالن ژوژه ی100ml-درپوش-ابفشان-قیف
ازمایش سوم:مایع در مایع(صورت ازمایش:محلول 0.1 مولار به حجم100ml Hcl باa=37% وd=1.19g/lit)
CM=0.01mol/lit
نحوه ی انجام محاسبات:
نحوه ی انجام ازمایش:
وسایل مورد نیاز:بشر-قاشقک-ترازو-بالن ژوژه ی100ml-همزن شیشه ای-ابفشان پلاستیکی
ازمایش دوم:جامد در مایع(صورت ازمایش:0.01 مولار Na2Co3 را به حجم 100mlبرسانید)
نحوه ی انجام محاسبات:
ابتدا تمام وسایل مورد نیاز در ازمایش را می شوییم و انها را کاملا با پارچه خشک می کنیم.اول در بشرml 150
نحوه ی انجام ازمایش:
وسایل مورد نیاز:بشر-قاشقک-ترازو-همزن شیشه ای-بالن ژوژه یml 50-درپوش-ابفشان پلاستیکی
محلول سازی(جامد در مایع-مایع در مایع)
گزارش کار شیمی عمومی(گروه 2 ساعت 1 الی 5)
فائزه پونکی
گزارش کار اول:اشنایی با قوانین ازمایشگاه ووسایل ازمایشگاهی
1.همواره با امادگی قبلی به ازمایشگاه امده و گزارش کار ازماشگاه را قبلا مطالعه کرده باشید.
2.قبل از برداشتن هر ماده برچسب روی شیشه را به دقت بخوانید.
3.از چشیدن یا لمس کردن مواد شیمیایی جدا خودداری کنید.
4.از بوییدن مستقیم مواد شیمیایی پرهیز کنید.
5.هر گاه اسید یا باز یا هر ماده ی شیمیایی خورنده یی روی میز یا زمین بریزد با مقدار زیادی اب بشویید.
6.از حرارت دادن وسایلی مثل استوانه مدرج و بالن پیمانه ای خودداری کنید چون براحتی میشکند.
7.میز ازمایشگاه را تمییز نگه دارید و هر گونه اشغال را به سطل زباله بریزید.
8.قبل از ترک ازمایشگاه لوازمی که از انها استفاده کردید بشویید و در جای مناسب قرار دهید.
و
.
.
.
مواظب خود باشید و به علایم درج شوده روی مواد و ابزارها دقت کنید!؟
اشنایی با ابزارهای ازمایشگاهی
ارلن:برای گرم کردن محلولها و مایع ها یا نگهداری انها و همچنین در سنجش حجمی بکار میرود.
کردن و نیز برای تهیه مواد گازی بکار میرود.
عینک پلاستیکی:برای محافظت چشم از پاشیده شدن اسیدها ابزها و سایر مواد خطرناک در ازمایشگاه.
هاون چینی:وسیاه ای برای خرد و نرم کردن مواد در ازمایشگاه.
لوله ی قیف دار:برای انتقال مایع از ظرفی به ظرف دیگر یا برای ریختن مایع یه محلولها بر روی مواد جامد(مثلا اضافه کردن اسید بر روی فلز ها)بکار میرود.
گیره ی چوبی:برای نگه داشتن لوله ی ازمایشگاه بکار می رود.
گیره ی بورت:گیره ایست فلزی که مستقیما به میله ی پایه ی فلزی وصل می شود و برای نگه داشتن بورت بکار می رود.
گیره ی بالن:گیره ایست فلزی برای نگه داشتن بالن ارلن و... به وسیله ی شاخک و پایه کاربرد دارد.
کپسول چینی:ظرفی است از نوع چینی که برای گرم و خشک کردن مواد یا گرفتن اب تبلور مواد بلوری بکار می رود.
قیف جدا کننده:برای جدا کردن دو مایع که با هم دیگر امیخته نشده باشد(اب و روغن)
قیف ساده:برای صاف کردن و نیز انتقال مایعها از ظرفی به ظرف دیگر است.
قطره چکان:برای برداشتن یا ریختن مایعهای سمی بکار می رود.از نوع مدرج ان به جای پیپت مدرج برای برداشتن حجم معینی از مایعها و محلولها بکار می رود.
قاشقک:وسیله ایست برای نرم کردن پودر و برداشتن ان.
شیشه ساعت:وسیله ای شیشه ای که معمولا برای تبخیر محلولها به منظور ایجاد بلوردر گرمای ملایم به کار می رود.
شعله پخش کن:برای پخش شعله ی چراغ گاز ازمایشگاه به منظور خم کردن و نرم کردن لولهای شیشه بکار میرود.
مثلث نسوز:وسیله ای است فلزی که روکشی ازچینی نسوز دارد و معمولا ان را روی سه پایه قرار می دهند و برای نگه داشتن بوته ی ازمایشگاهی و نظایر ان بکار می رود.
سه پایه فلزی:وسیله ای است برای نگه داشتن وسایل و گرم کردن انها در بالای شعله گازبکار می رود.
دستگاه خنک کننده(دیسکاتور):وسیله ی شیشه ای که در قسمت پایین ان ماده ی نم گیری مانند سولفوریک اسید غلیظ می ریزند و در بالای ان یک صفحه ی مشبک چینی ماده ی خشک شدنی مایع یا جامد را قرار می دهند.
چراغ گاز :وسیله فلزی گازی است که برای گرما دادن به مواد و نظایر ان به کار می رود.
توری نسوز:نوعی توری فلزی است که در قسمت وسط ان نوعی ماده ی نسوز قرار داده شده که برای جلوگیری از تاثیر مستقیم شعله بر انچه باید به وسیله ی شعله گرم شود به کار می رود.
ابفشان پلاستیکی:برای نگه داشتن اب مقطریا محلولها و مایعهای دیگر و ریختن مقدار کم انها به کار می رود.
پنس فلزی:برای برداشتن و گذاشتن وزنهای ترازو به کار می رود.
پیپت مدرج:برای برداشتن مقدار معین یا دلخواه از مایع یا محلولها در مقیاس نسبتا کم به ویژه در سنجش حجمی به کار می رود.
پیپت حبابدار:برای برداشتن یا ریختن مقدار مشخص از محلولها یا مایعها به ویژه در سنجشهای حجمی بکار می رود.
بورت مدرج:کار ویژه ی ان در سنجشهای حجمی است.معمولا محلولی که غلظت ان مشخص است در ان میریزند.
بوته چینی:وسیله ای چینی است که برای گرما دادن شدید و تجزیه کردن مواد جامد در دمای چراغ گاز یا کوره ی الکتریکی در ازمایشگاه استفاده کرد.
بشر:برای گرم کردن محلولها یا مایعها در سنجشهای حجمی(مثلا سنجش اسید و باز)به کار می رود.ار نوع مدرج ان می توان برای برداشتن حجم معین ویا تعیین حجم محلولها یا مایع ها البته به طور تقریبی استفاده کرد.
بالن ته گرد:برای گرم کردن محلولها یا مایعها به ویژه برای عمل تقطیر از ان استفاده کرد.
بالن ته پهن:برای نگه داشتن محلولها نیز برای درست کردن ابفشان از ان استفاده میشود.برای گرم کردن نباید استفاده کرد چون پیرکس نیست.
بالن پیمانه ای(بالن ژوژه):کار ویژه ی ان در تهیه محلولهای سنجیده با غلظت معین است.
بالن با لوله جانبی:وسیله ای مخصوص تقطیر است(می توان به جای ارلن تخلیه از ان استفاده کرد اما شکننده تر از ان است)
استوانه ی مدرج:برای برداشتن حجم معین یا تعیین حجم ماع ها و محلولها نیز در تعیین حجم مواد جامد و چگالی انها(به وسیله ی ترازو) به کار می رود.میزان دقت ان از ارلن ا بشر مدرج بیشتراما از بورت یا پیپت مدرج کمتر است.
ارلن تخلیه:برای ایجاد خلا به وسیله ی خرطوم ابی در ازمایشگاه به منظور سرعت بخشیدن به عمل صاف
اشنایی با قوانین و مقررات:
 آمار
وب سایت:
آمار
وب سایت:

